La espectroscopia ultravioleta-visible-infrarroja cercana (UV-Vis-NIR) es una técnica utilizada para determinar las propiedades ópticas (reflectancia, absorbancia y transmitancia) de líquidos y sólidos. Se utiliza con frecuencia en una amplia gama de aplicaciones, incluidas las farmacéuticas, de alimentos y bebidas, químicas, educativas, etc.
El día de hoy nos enfocaremos en hablar de los conceptos básicos, su funcionamiento y algunos modelos que podrían interesarte.
La cuestión de si la luz es una onda o una partícula, a lo largo de la historia, ha sido objeto de mucho debate. Es bien sabido que se desarrollaron varias teorías a partir de la afirmación de Newton de que la luz es una partícula y de la afirmación de Huygen de que la luz es una onda. En la física moderna ahora se sabe que; Si bien la luz tiene naturaleza ondulatoria, también tiene propiedades similares a las de partículas. En este artículo, describiremos la naturaleza dual de la luz y la relación entre materia y absorbancia de la luz.
1. La naturaleza dual de la luz
1.1 Propiedades ondulatorias de la luz
Aunque generalmente se dice que la luz es una onda, a diferencia de las ondas que se producen en la superficie de una masa de agua, no requiere un medio. Como se muestra en la figura 1, la luz consta de un campo eléctrico y un campo magnético que se cruzan entre sí en ángulo recto a medida que se mueven a través del vacío. La distancia entre picos sucesivos del campo eléctrico o del campo magnético es la longitud de onda.
Al manipular la luz, nos encontramos con fenómenos propios de las ondas, como la interferencia y la difracción. Es bien conocido el experimento en el que Young descubrió la interferencia de la luz y concluyó que la luz era una forma de onda. Como se muestra en la figura 2, la luz monocromática emitida por una fuente de luz, L, pasa a través de una única rendija y luego pasa a través de dos rendijas más, S 1 y S 2 . Como resultado, en la parte posterior de la pantalla se observan franjas de interferencia como un patrón de franjas alternas de brillo y oscuridad. Esto se puede explicar pensando en S 1 y S 2 como fuentes de luz en fase entre sí. Las ondas viajan desde estas fuentes de luz hasta la pantalla en la parte posterior. En los puntos donde las ondas están en fase, se refuerzan entre sí, mientras que en los puntos donde las ondas están desfasadas, se anulan entre sí. Si uno piensa en la superficie de este papel como la superficie de una masa de agua, y las rendijas como particiones con agujeros, entonces las ondas que se mueven de izquierda a derecha se comportarían de la misma manera. En este sentido, el experimento de Young demuestra de forma intuitiva la naturaleza ondulatoria de la luz. Por cierto, la rejilla de difracción utilizada en un espectrofotómetro UV-VIS crea luz monocromática utilizando la naturaleza ondulatoria que la luz difracta y causa interferencia.
La luz se compone de ciertos tipos de ondas electromagnéticas las cuales reciben diferentes nombres según su longitud de onda, como se muestra en la Fig.3. "Luz" normalmente se refiere a ondas electromagnéticas en el rango que abarca la radiación infrarroja y la radiación ultravioleta, pero en algunos casos se refiere sólo a la luz visible. La luz con longitudes de onda en un rango de aproximadamente 400 a 800 nm se denomina "luz visible" y es la luz que los humanos podemos ver a simple vista. Por ejemplo, la luz con una longitud de onda de 470 nm es azul, la luz con una longitud de onda de 540 nm es verde y la luz con una longitud de onda de 650 nm es roja. La luz visible podría describirse como el tipo de luz con la que los humanos estamos familiarizados debido a nuestra capacidad de verla.
1.2 Propiedades de la luz similares a las partículas
A continuación, observemos el comportamiento de la luz como partícula. Entre los avances que ayudaron a identificar este comportamiento se encuentran una serie de experimentos sobre el efecto fotoeléctrico que se llevaron a cabo a finales del siglo XIX y principios del XX. Los resultados de estos experimentos no podían explicarse considerando la luz como una onda, pero sí podían explicarse considerándola como una partícula. Cuando se enfatizan los aspectos de la luz similares a partículas, se utiliza el término "fotón".
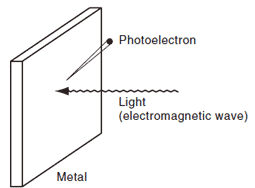
Fig.4 Concepto de efecto fotoeléctrico 3)
La figura 4 ilustra el concepto básico del efecto fotoeléctrico, un fenómeno en el que se emiten electrones desde una superficie metálica cuando la luz incide sobre ella. Los electrones emitidos se denominan "fotoelectrones". Aunque no se emiten electrones cuando una luz intensa incide sobre la superficie, sí se emiten electrones cuando una luz de longitud de onda más corta incide sobre la superficie. Si la longitud de onda de la luz que incide sobre la superficie disminuye, el número de electrones emitidos no cambia, pero la energía de los electrones aumenta. Si la luz que incide sobre la superficie se intensifica, el número de electrones emitidos aumenta, pero la energía de los electrones permanece igual. Estos fenómenos no se pueden explicar considerando la luz como una onda, pero sí se pueden explicar considerándola como una partícula, y estas partículas eliminan los electrones cuando golpean el metal. En combinación con los resultados de los experimentos sobre el efecto Compton y otros experimentos, se reconocieron las propiedades similares a las de las partículas. Por cierto, el tubo fotomultiplicador que se utiliza como detector en los espectrofotómetros UV-VIS detecta la luz mediante el efecto fotoeléctrico.
Hemos analizado la naturaleza dual de la luz, con su mezcla de propiedades ondulatorias y partículares. El hecho de que la luz tenga estas dos características opuestas puede parecer extraño, pero así es como se modela la luz en la física moderna.
2. Absorción de luz por la materia
Se puede obtener una amplia variedad de información sobre una sustancia irradiándola con luz. Con un espectrofotómetro UV-VIS, irradiar una sustancia con luz ultravioleta y visible permite obtener información sobre los electrones de esa sustancia, e incluso es posible medir su cantidad.
Consideremos la absorción de luz por la materia. Esto está estrechamente relacionado con la mecánica cuántica. La teoría de la mecánica cuántica se desarrolló a principios del siglo XX y forma parte de la base de la física moderna. La mecánica cuántica se puede entender fácilmente comparándola con la mecánica newtoniana.
En términos generales, la mecánica newtoniana es una teoría que se relaciona con el movimiento de partículas grandes, mientras que la mecánica cuántica es una teoría que se relaciona con el movimiento de partículas pequeñas (por ejemplo, átomos y moléculas). La mecánica newtoniana maneja el movimiento de las partículas como una entidad continua, mientras que la mecánica cuántica afirma que las partículas pequeñas existen en estados discretos de movimiento (energías). En la época en que la mecánica newtoniana era la teoría dominante, el concepto de mecánica cuántica era difícil de aceptar para la gente. Sin embargo, con el tiempo se demostró su validez.
Conoce nuestro catálogo
de UV-Vis
La mejor tecnología para ti, si te interesó alguno de nuestros productos escríbenos al correo jnacianceno@analitek.com o mandanos un Whastapp 8119110305
Resolver las ecuaciones de la mecánica cuántica que se relacionan con los electrones de un átomo da un modelo, como el que se muestra en la figura 5, en el que los electrones tienen estados de energía discretos. E 0 se denomina "estado fundamental" y E 1 , E 2 , etc., se denominan "estados excitados". Para que un electrón cambie de E 0 a E 1 , una luz con una energía de (E 1 - E 0 ) debe incidir sobre el electrón. Esta es la "absorción" de la luz. Los electrones tienen niveles de energía particulares y los rayos de luz ultravioleta y visible tienen la energía para cambiar los estados energéticos de los electrones.
Debido a que el estado de mayor energía, E 1 , es inestable, el electrón pronto regresa al estado fundamental, E 0 . La energía descargada cuando el electrón regresa de E 0 a E 1 (E 1 - E 0 ) se convierte en calor. Si por alguna razón no se convierte en calor, la energía se descarga en forma de luz. El fenómeno de la emisión de luz es bien conocido como fluorescencia o fosforescencia.
En relación con la medición cuantitativa realizada con espectroscopía, la consecuencia de este fenómeno es que hay una gran cantidad de absorción si existe una gran cantidad de moléculas objetivo en una solución, y solo una pequeña cantidad de absorción si solo hay una pequeña cantidad de moléculas objetivo. moléculas objetivo.
Obtener la cantidad y, por tanto, la concentración de una sustancia a partir del grado de absorción es el principio fundamental de la medición cuantitativa.
El gráfico obtenido utilizando el eje horizontal para representar la longitud de onda y el eje vertical para representar el grado de absorción se denomina "espectro de absorción". El grado de absorción se expresa en términos de la unidad de "absorbancia" (Abs). La Fig.6 muestra un espectro de absorción de la solución de β-caroteno obtenida con el espectrofotómetro UV-VIS Shimadzu UV-2550 (Fig.7). El β-caroteno es la sustancia principal de las zanahorias que les da su color. Como se muestra en la Fig. 6, se absorbe principalmente luz azul y violeta de longitudes de onda en el rango de 400 a 500 nm. Debido a que la luz visible que llega al ojo del observador consiste en una mezcla de los componentes verdes y rojos que sobran, las zanahorias, que contienen una gran cantidad de β-caroteno, parecen tener un color amarillo-rojo.
3. Resumen
Aquí hemos analizado las propiedades de la luz y la forma en que se absorbe, dos aspectos fundamentales del funcionamiento de un espectrofotómetro UV-VIS. En el campo de la espectroscopia, además de los espectrofotómetros UV-VIS, existen otros tipos de dispositivos de medición espectroscópica, como los espectrofotómetros de infrarrojos, los fotómetros de absorción atómica, los espectrofotómetros Raman y los espectrofotómetros de fluorescencia, todos los cuales realizan distintos tipos de análisis. El uso selectivo de estos dispositivos permite obtener varios tipos de información sobre muestras desde diferentes perspectivas. En el próximo volumen, describiremos la estructura de un espectrofotómetro UV-VIS.
Referencias:
- 1) Kanji Kihone: Medición de la luz, Capítulo 10
(Editado por el Instituto de Ingeniería de Iluminación de Japón, Publicado por Nippon Riko Shuppankai, 1993), p. 172 - 2) Akira Harajima: Mecánica cuántica elemental
(Shokabo, 1987), pág. 3 - 3) Ryuzo Abe: Introducción a la mecánica cuántica
(Iwanami Shoten, Publishers, 1987), pág. 31
¿cómo podemos ayudarte el día de hoy?
Trabajemos juntos para lograr un mundo mejor, háblanos de tu proyecto.